عنوان:
Based on gene expression profiling and systems miR-28-5p regulates the expression level of GLUD1 gene in multiple sclerosis patients: a study biology analyses
تاریخچه بیماری بیماری ام اس:
یکی از نخستین گزارشها مربوط به زن جوانی به نام «هالدورا» است که در قرن دوازدهم میلادی در ایسلند میزیسته. او بهطور ناگهانی بینایی و توان حرکتی خود را از دست داد، اما پس از هفت روز و اعتراف به قدیس ها، این تواناییها را بازیافت. نمونهای دیگر، «قدیس لیدوینا اهل اسخیدام» است؛ راهبهای اهل هلند که بین سالهای 1380 تا 1433 میلادی میزیسته. او از سن 16 سالگی تا زمان مرگ در 53 سالگی دچار علائمی مانند دردهای دورهای، ضعف اندام تحتانی و کاهش بینایی بوده است؛ علائمی که با نشانههای اماس مطابقت دارند. این گزارشها از بروز علائم مشابه در جوامع اسکاندیناوی و شمال اروپا، منجر به شکلگیری فرضیهای با عنوان «ژن وایکینگ» برای تبیین گسترش جغرافیایی بیماری اماس شده است
مقدمه:
ام اس (مولتیپل اسکلروزیس) یک اختلال خودایمنی مزمن سیستم عصبی مرکزی (CNS) است که با آسیب به غلاف میلینِ نورونها در مغز، نخاع و عصب بینایی شناخته میشود. این آسیبِ دیمیلیناسیون، انتقال سیگنالهای عصبی را مختل کرده و منجر به طیف گستردهای از علائم بالینی نظیر اختلالات بینایی، ضعف عضلانی، ناهماهنگی حرکتی، اختلالات حسی و گاهی مشکلات شناختی یا عاطفی می گردد. شیوع این بیماری عمدتاً در افراد 20 تا 40 سال مشاهده میشود، هرچند امکان بروز در هر سنی وجود دارد. مطالعات نشان می دهد زنان 2 تا 3 برابر بیش از مردان در معرض ابتلا هستند.
علل و عوامل خطر:
علت دقیق بیماری ام اس ناشناخته است، اما شواهد قوی از نقش سیستم ایمنی در ایجاد التهاب و تخریب میلین حمایت می کنند. در این بیماری، لنفوسیتهای T خودواکنشگر به طور غیرطبیعی به غلاف میلینِ نورون ها حمله کرده و پلاک های اسکلروزیس (زخم های بافتی) ایجاد می کنند. این فرآیند احتمالاً تحت تأثیر ترکیبی از عوامل ژنتیکی و محیطی است:
• ژنتیک:
وجود سابقه خانوادگی ام اس، خطر ابتلا را افزایش میدهد.
• عوامل محیطی:
کمبود ویتامینD: ارتباط معناداری بین سطح پایین ویتامین D (ناشی از کاهش مواجهه با نور خورشید) و افزایش خطر ام اس گزارش شده است.
عفونتهای ویروسی: ویروس اپشتین بار (EBV) به عنوان یک محرک احتمالی در فعالسازی پاسخ ایمنی غیرطبیعی مطرح است.
سیگار: مصرف دخانیات با تشدید التهاب سیستمیک، پیشرفت بیماری را تسریع میکند.
بیان آمار:
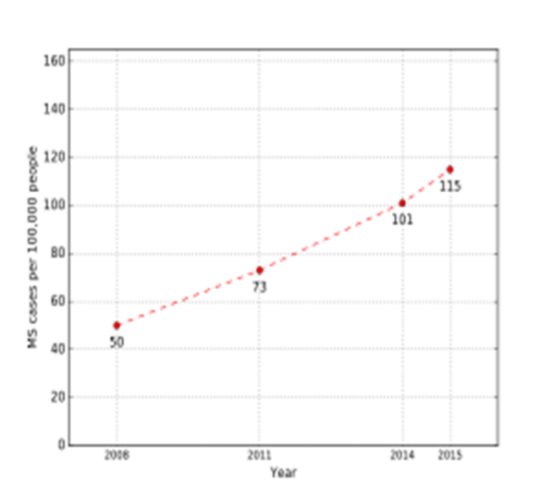
بر اساس داده های اپیدمیولوژیک، ایران بالاترین نرخ شیوع ام اس را در منطقه خاورمیانه دارد. مطالعات نشان می دهد بین سالهای 2008 تا 2015 ، تعداد مبتلایان به ازای هر 100٬000 نفر جمعیت روند افزایشی چشمگیری داشته است. این افزایش ممکن است با تغییر سبک زندگی، بهبود روش های تشخیصی یا عوامل محیطی نظیر آلودگی هوا و کاهش سطح ویتامین D مرتبط باشد. برنامه های ملی غربالگری و آموزش عمومی درباره علائم اولیه ام اس، به ویژه در گروه های پرخطر، از اولویتهای نظام سلامت ایران است.
فرایند از بین رفتن میلین (غلاف چربی روی اعصاب) در بیماری ام اس. حضور گلبولهای سفید و ایجاد پلاک در عکس مشهود است.

ژنتیک
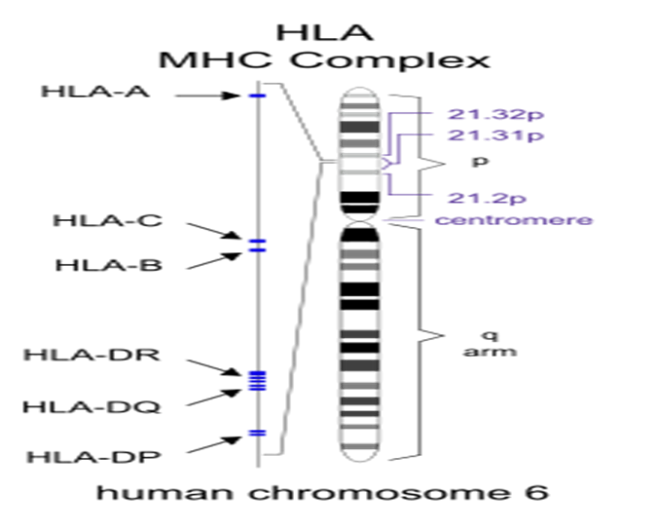
بهطور کل تخمین زده میشود که تغییرات HLA دلیل 20 تا 60 ٪ از استعداد ژنتیکی میباشد.روشهای نوین ژنتیک (مطالعه ارتباطی تمام ژنومی) باعث کشف دوازده ژن دیگر بیرون از جایگاه کروموزومی HLA شدهاست که احتمال ابتلاء به اماس را افزایش میدهد.
HLA region of Chromosome 6. Changes in this area increase the probability of getting Ms
علت بیماری ام اس: نقش عوامل ژنتیکی
اگرچه ام اس بهعنوان یک بیماری کاملاً ارثی طبقهبندی نمیشود، اما شواهد قوی از تأثیر تنوعهای ژنتیکی در افزایش استعداد ابتلا به این بیماری حمایت میکنند. مطالعات اپیدمیولوژیک نشان میدهد احتمال بروز ام اس در بستگانِ درجهیکِ افراد مبتلا بهطور معناداری بالاتر از جمعیت عمومی است. این الگوی خطر بهویژه در دوقلوهای همسان مشهود است:
• دوقلوهای همسان: در 30 % موارد، هر دو قل به ام اس مبتلا میشوند.
• دوقلوهای غیرهمسان: نرخ هم ابتلایی به 5 % کاهش مییابد.
• خواهر و برادرها: خطر مشترک حدود 5/2 % است.
ژنتیک ام اس: از HLA تا مطالعات ژنومیک
۱. نقش کلیدی ناحیه HLA:
ناحیه HLA (Human Leukocyte Antigen) روی کروموزوم 6، مسئول کدکردن مولکولهای اصلی سازگاری بافتی (MHC) است که در تنظیم پاسخ ایمنی نقش دارند.
• تغییرات در این ناحیه (بهویژه آللهای خاصی مانند HLA-DRB1*15:01) عامل 20 تا 60 % از استعداد ژنتیکی به ام اس محسوب میشوند.
۲. کشف ژنهای جدید با مطالعات GWAS
• روشهای مطالعه ارتباطی تمام ژنومی (Genome-Wide Association Studies; GWAS)، 12 لوکوس ژنی خارج از ناحیه HLA را شناسایی کردهاند که با افزایش خطر ام اس مرتبطند.
• این ژنها عمدتاً در مسیرهای التهابی، تنظیم ایمنی (مانند IL2RA، IL7R) و حفاظت از میلین نقش دارند.
گستره شیوع
الگوی جغرافیایی شیوع ام اس
ام اس بهطور کلی در مناطق با عرض جغرافیایی بالا (دور از استوا) شیوع بیشتری دارد. این الگو احتمالاً با عوامل محیطی مانند کاهش مواجهه با نور خورشید و سطوح پایین ویتامین D مرتبط است. با این حال، استثنائات قابل توجهی در این الگو مشاهده میشود:
• گروههای قومی با شیوع پایین در مناطق دور از استوا:
o سامی (اقوام ساکن اسکاندیناوی و روسیه)، سرخپوستان آمریکایی، هاتِریتهای کانادا، مائوری نیوزیلند و اینوئیتهای کانادا.
• گروههای قومی با شیوع بالا در مناطق نزدیک به استوا:
o ساردنیها (ساکن جزیره ساردینیا ایتالیا)، فلسطینیها و پارسیان هند.
این تناقضات نشان میدهد که علاوه بر عرض جغرافیایی، تعامل پیچیده ژنتیک و محیط در بروز ام اس نقش کلیدی دارد.
علائم و نشانههای بالینی ام اس
ام اس طیف وسیعی از علائم عصبی را ایجاد میکند. این علائم بهطور کلی در چهار دسته اصلی طبقهبندی میشوند:
1. علائم حسی-حرکتی
• اختلالات حسی: خوابرفتگی، گزگز و مورمور، کاهش حس لمس یا دردهای نوروپاتیک.
• ناهنجاریهای حرکتی:
o ضعف عضلانی (اغلب در اندام تحتانی)
o اسپاسم و گرفتگی عضلات
o لرزش و ناهماهنگی حرکتی (آتاکسی)
o کاهش تعادل و هماهنگی
۲. علائم بینایی
• نوریت اپتیک (التهاب عصب بینایی) با علائمی مانند:
o کاهش دید یا تاری دید
o دوبینی
o حرکات غیرارادی چشم
۳. اختلالات سیستم خودگردان (اتونوم)
• مشکلات مثانه: بیاختیاری یا احتباس ادرار
• اختلالات روده: یبوست یا بیاختیاری مدفوع
• اختلال عملکرد جنسی
۴. علائم عمومی و سایر موارد
• خستگی مزمن (شایعترین علامت)
• اختلالات گفتاری (کندی گفتار)
• دردهای حاد یا مزمن (مانند درد صورت)
• مشکلات شناختی (کاهش حافظه یا تمرکز)
نشانه های ام اس:
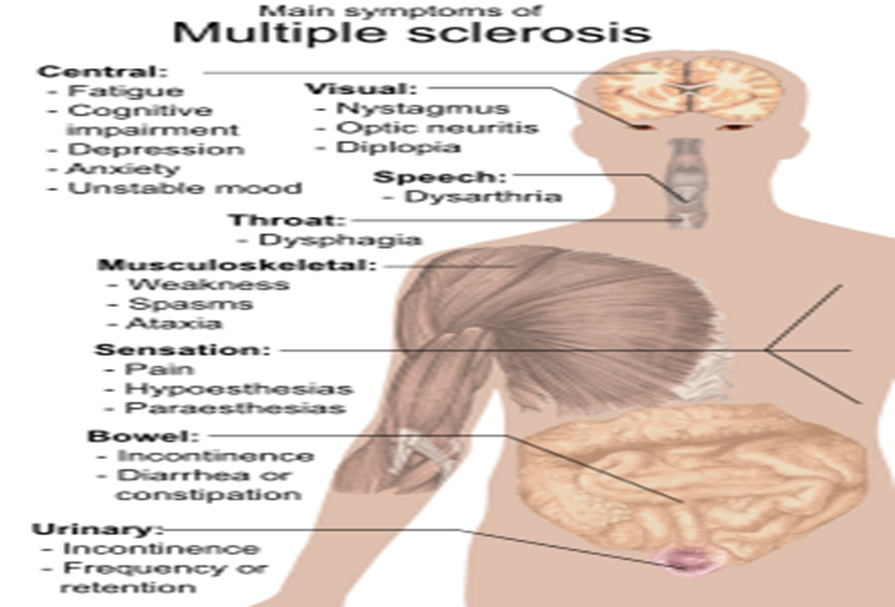
جزئیات تصویر ضایعات بیماری اماس در ساقه مغز و ستون فقرات
مواد و روش ها
بیان (GEO) و سپس توسط GEO2R برای یافتن ژن های بیان شده متفاوت توسط gse21924 مورد تجزیه و تحلیل قرار گرفت. این ژن از سایت دیوید در بخش kegg-pathway انتخاب شد. در مرحله بعد از سایت mir-walk ژن مورد نظر استفاده کرده و miR را انتخاب می کنیم. در سایت DIANA Tool قسمت miRNA-IncRNA را انتخاب می کنیم و miR مورد نظر را جستجو می کنیم. مرحله بعدی بررسی رابطه بین ژن های lnc است، از سایت lncRRISEARCH استفاده کنید. در نهایت از سایت kegg مسیر سیگنال دهی که ژن مورد نظر در آن درگیر است را پیدا می کنیم و از محل رشته وارد ژن مورد نظری که انتخاب کرده ایم می شود و سپس پروتئین های مربوط به آن را به ما می دهد.

Figure 1. The miRNA-mRNA interaction analysis, based on miRWalk online database.
یافته ها
GLUD1، می تواند پیشرفت مولتیپل اسکلروزیس را به عنوان یک mRNA با بیان بالا در بیماران تنظیم کند.
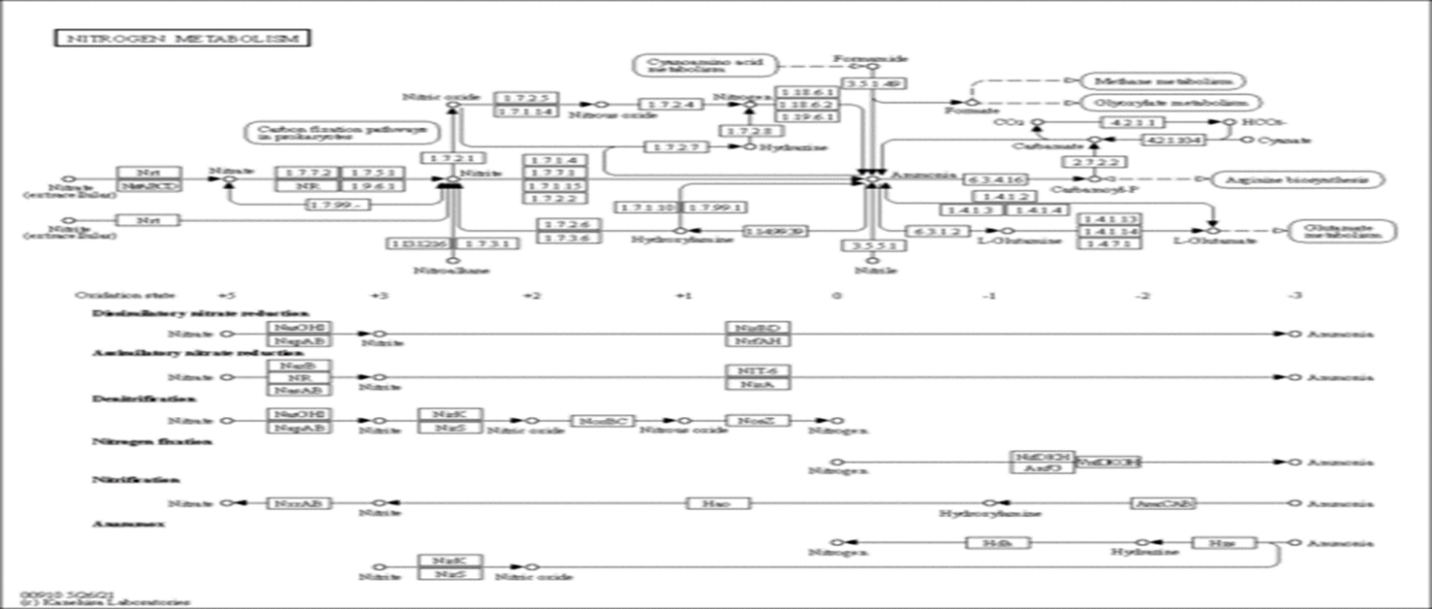
MiR-28a-5p lncRNA A1BG-AS1 سطح بیان GLUD1 را در تنظیم مسیرهای سیگنالینگ متابولیسم تنظیم می کند. بر اساس آنالیز برهمکنش پروتئین-پروتئین، پروتئینهای GPT2 و GLS2 برهمکنش قابلتوجهی با پروتئینهای GLUD1 دارند که میتوانند وضعیت بیماری ام اس را با تعدیل مسیر سیگنالدهی متابولیسم نیتروژن تنظیم کنند.
Figure 2. Nitrogen metabolism signaling pathways
نتیجه گیری
(miR-28-5p نام یک نوع میکروRNA ) و lncRNA A1BG-AS1 (نام یک نوع میکرو RNA) سطح بیان GLUD1 را در تنظیم مسیرهای سیگنالینگ متابولیسم در بیماران مبتلا به مولتیپل اسکلروزیس تنظیم می کنند. بیان بالای پروتئین GLUD1 خطر ابتلا به مولتیپل اسکلروزیس را افزایش می دهد و miR-28-5p و lncRNA A1BG-AS1 می توانند این اختلال را کنترل کنند.
درمان های جایگزین
بیش از 50 % افراد مبتلا به اماس ممکن است از درمانهای مکمل یا جایگزین استفاده کنند، با این حال درصد این افراد بسته به چگونه تعریف شدن درمان جایگزین متغیر خواهد بود. شواهدی در خصوص مؤثر بودن درمانهای این چنین در غالب موارد یا ضعیف است یا اینکه وجود ندارد. در حالی که شواهد غیر قطعی وجود دارد که ویتامین دی در درمان این بیماری مؤثر است، با این حال شواهد کافی برای نتیجهگیری قطعی موجود نیست.
: References
1. Kemppinen AK, Kaprio J, Palotie A, Saarela J. Systematic review of genome-wide expression studies in multiple sclerosis. BMJ Open 2011 Jul 18;1(1):e000053. PMID: 22021740
2. B.T. Sherman, M. Hao, J. Qiu, X. Jiao, M.W. Baseler, H.C. Lane, T. Imamichi and W. Chang. DAVID: a web server for functional enrichment analysis and functional annotation of gene lists (2021 update). Nucleic Acids Research. 23 March 2022. doi:10.1093/nar/gkac194.
3. Sticht C, De La Torre C, Parveen A, Gretz N.: miRWalk: An online resource for prediction of microRNA binding sites. PLoS One. 2018 Oct 18;13(10)
4. Dimitra Karagkouni, Maria D Paraskevopoulou, Spyros Tastsoglou, Giorgos Skoufos, Anna Karavangeli, Vasilis Pierros, Elissavet Zacharopoulou, Artemis G Hatzigeorgiou, DIANA-LncBase v3: indexing experimentally supported miRNA targets on non-coding transcripts, Nucleic Acids Research, DOI: 10.1093/nar/gkz1036
5. Maria D. Paraskevopoulou, Dimitra Karagkouni, Ioannis S Vlachos, Spyros Tastsoglou, Artemis G Hatzigeorgiou, microCLIP super learning framework uncovers functional transcriptome-wide miRNA interactions, Nature communications, DOI:10.1038/s41467-018-06046-y
6. LncRRIsearch: a web server for lncRNA-RNA interaction prediction integrated with tissue-specific expression and subcellular localization data
7. Kanehisa M, Goto S. KEGG: kyoto encyclopedia of genes and genomes. Nucleic Acids Res. 2000 Jan 1;28(1):27-30. doi: 10.1093/nar/28.1.27. PMID: 10592173; PMCID: PMC102409a
نویسنده: فائزه رضایی، کارشناسی ارشد زیست شناسی سلولی و مولکولی
تاریخ انتشار :
1404/03/13
کد :
46096
تعداد بازدید:
1137